บทที่ 2 อะตอมเเละสมบัติของธาตุ
2.1 เเบบจำลองอะตอม
อะตอมมีขนาดเล็กมากและมองไม่เห็นด้วยตาเปล่า แบบจำลองของอะตอมจึงมีวิวัฒนาการดังนี้
2.1.1 แบบจำลองอะตอมของจอร์น ดอลตัน

ในปี พ.ศ. 2346 (ค.ศ. 1803) จอห์น ดอลตัน (John Dalton) นักวิทยาศาสตร์ชาวอังกฤษได้เสนอทฤษฎีอะตอมเพื่อใช้อธิบายเกี่ยวกับการเปลี่ยนแปลงของสารก่อนและหลังทำปฏิกิริยา รวมทั้งอัตราส่วนโดยมวลของธาตุที่รวมกันเป็นสารประกอบ ซึ่งสรุปได้ดังนี้
1) ธาตุประกอบด้วยอนุภาคเล็กๆหลายอนุภาคเรียกอนุภาคเหล่านี้ว่า “อะตอม” ซึ่งแบ่งแยกและทำให้สูญหายไม่ได้
2) อะตอมของธาตุชนิดเดียวกันมีสมบัติเหมือนกัน แต่จะมีสมบัติ แตกต่างจากอะตอมของธาตุอื่น
3) สารประกอบเกิดจากอะตอมของธาตุมากกว่าหนึ่งชนิดทำปฏิกิริยา เคมีกันในอัตราส่วนที่เป็นเลขลงตัวน้อยๆ
จอห์น ดอลตัน ชาวอังกฤษ เสนอทฤษฎีอะตอมของดอลตัน
- อะตอมเป็นอนุภาคที่เล็กที่สุด แบ่งแยกอีกไม่ได้
- อะตอมของธาตุชนิดเดียวกันมีสมบัติเหมือนกัน
- อะตอมต้องเกิดจากสารประกอบเกิดจากอะตอมของธาตุตั้งแต่ 2 ชนิดขึ้นไปมารวมตัวกัน ทางเคมี
ทฤษฎีอะตอมของดอลตันใช้อธิบายลักษณะและสมบัติของอะตอมได้เพียงระดับหนึ่ง แต่ต่อมานักวิทยาศาสตร์ค้นพบข้อมูลบางประการที่ไม่สอดคล้องกับทฤษฎีอะตอมของ ดอลตัน เช่น พบว่าอะตอมของธาตุชนิดเดียวกันอาจมีมวลแตกต่างกันได้
ลักษณะแบบจำลองอะตอมของดอลตัน

ลักษณะอะตอมเป็นทรงตันขนาดเล็ก ที่สร้างขึ้นใหม่หรือทำลายไม่ได้ เปรียบเสมือนลูกเปตอง
- ทำไมอะตอมต่างชนิดกัน จึงไม่เหมือนกัน
- ทำไมอะตอมต่างๆ จึงทำปฏิกิริยากับบางธาตุเท่านั้น
- อะตอมรวมกันเกิดสารประกอบได้อย่างไร มีเเรงยึดเหนี่ยวอย่างไร
- ทำไมอะตอมชนิดเดียวกันจึงมีคุณสมบัติเเตกต่างกัน
เป็นเครื่องที่ใช้ทดลองเกี่ยวกับการนำไฟฟ้าโดยหลอดรังสีแคโทดจะมีความดันต่ำมาก และความต่างศักย์สูงมาก วิลเลียม ครูกส์ได้สร้างหลอดรังสีแคโทดขึ้นมาโดยใช้แผ่นโลหะ 2 แผ่นเป็นขั้วไฟฟ้า โดยต่อขั้วไฟฟ้าลบกับขั้วลบของเครื่องกำเนิดไฟฟ้าเรียกว่า แคโทด และต่อขั้วไฟฟ้าบวกเข้ากับขั้วบวกของเครื่องกำเนิดไฟฟ้าเรียกว่า แอโนด
หลอดรังสีเเคโทดมีส่วนประกอบดังนี้
1) ขั่วเเคโทด (Cathode)
2) ขั่วเเอโนด (Anode)
3) เครื่องวัดกระเเสไฟฟ้า
4) เครื่องกำเนิดไฟฟ้าศักย์สูง

สมบัติของรังสีเเคโทด
การค้นพบอิเล็กตรอน
เซอร์โจเซฟ จอห์น ทอมสัน ดัดแปลงหลอดรังสีใหม่ ดังรูป





ผลการทดลองของโกสไตน์
เมื่อผ่านกระแสไฟฟ้า ปรากฏว่ามีจุดสว่างเกิดขึ้นทั้งฉากเรืองแสง ก. และฉากเรืองแสง ข.
โกลสไตน์ได้อธิบายว่า จุดเรืองแสงที่เกิดขึ้นบนฉากเรืองแสง ก. จะต้องเกิดจากที่ประกอบด้วยอนุภาคที่มีประจุไฟฟ้าบวก เคลื่อนที่ผ่านรูตรงกลางของแคโทด ไปยังฉากเรืองแสง แต่ยังไม่ทราบว่ารังสีที่มีประจุไฟฟ้าบวกนี้เกิดจากอะตอมของก๊าซ หรือเกิดจากอะตอมของขั้วไฟฟ้า และมีลักษณะเหมือนกันหรือไม่

อะตอมเป็นทรงกลมประกอบด้วยอนุภาคที่มีประจุบวก (โปรตอน) เเละอนุภาคที่มีประจุลบ (อิเล็กตรอน) กระจายอยู่ทั่วไปอะตอมในสภาพที่เป็นกลางทางไฟฟ้า โดยจะมีจำนวนประจุบวกเท่ากับประจุลบ
2.1.3 เเบบจำลองอะตอมของรัทเทอร์ฟอร์ด


ผลการทดลอง สรุปได้ดังนี้
• จุด X เป็นจุดที่อนุภาคแอลฟาผ่านไปยังฉากในแนวเส้นตรง แสดงว่า ภายในอะตอมน่าจะมีพื้นที่ว่างเป็นจำนวนมาก เพราะ อนุภาคแอลฟาส่วนใหญ่ทะลุผ่านแผนทองคำเป็นแนวเส้นตรง
• จุด Y อนุภาคแอลฟาเบี่ยงเบนเล็กน้อย แสดงว่าภายในอะตอมควรมีอนุภาคบางอย่างรวมกันเป็นกลุ่มก้อนขนาดเล็ก มีมวลมากพอที่ทำให้อนุภาคแอลฟาวิ่งไปเฉียดแล้วเบี่ยงเบน

• จุด Z อนุภาคแอลฟาสะท้อนกลับ แสดงว่าในอะตอมจะมีอนุภาคบางอย่างที่เป็นกลุ่มก้อน มีทวลมากพอที่ทำให้อนุภาคแอลฟาสะท้อนกลับ

การค้นพบนิวตรอน
สาเหตุที่ค้นพบนิวตรอน
1) เนื่อจากมวลของอะตอมต่าง มักเป็น 2 เท่า หรือมากกว่า 2 เท่าของมวลโปรตรอนรวมรัทเทอร์ฟอร์ดสันนิษฐานว่า น่าจะมีอนุภาคอีกชนิดหนึ่งอยู่ในนิวเคลียส และอนุภาคนี้ต้องมีมวลใกล้เคียงกันกับมวลของโปรตรอนมาก และต้องเป็นกลางทางไฟฟ้า
2) ทอมสันศึกษาหามวลของอนุภาคบวกของ Ne ปรากฎว่า อนุภาคบวกนี้มีมวล 2 เท่า ผลการทดลองนี้สนับสนุนว่าจะต้องมีอนุภาคอีกชนิดหนึ่งอยู่ในนิวเคลียสเชดวิก ได้ยิงอนุภาคแอลฟาไปยัง Be ปรากฎว่าได้อนุภาคชนิดนึ่งออกมาซึ่งมีมวลใกล้เคียงกับมวลของโปรตรอนและไม่มีประจุไฟฟ้า เรียกอนุภาคนี้ว่า "นิวตรอน"


สเปกตรัมแม่เหล็กไฟฟ้าประกอบด้วยคลื่นแม่เหล็กไฟฟ้าที่มีความยาวคลื่นต่าง ๆ กัน และมีความถี่ต่อเนื่องกันเป็นช่วงกว้าง มีทั้งที่มองเห็นได้และมองไม่เห็น มีชื่อเรียกต่าง ๆ กัน แสงที่ประสาทตาของมนุษย์สามารถรับรู้ได้เรียกว่า แสงที่มองเห็นได้ (visible light) มีความยาวคลื่นอยู่ในช่วง400–700 นาโนเมตร ซึ่งประกอบด้วยแสงสีต่าง ๆ กัน แต่ประสาทตาของมนุษย์ไม่สามารถแยกแสงที่มองเห็นเป็นสีต่าง ๆ ได้เอง ทำให้มองเห็นสีรวมกัน ซึ่งเรียกว่า แสงขาว (white light) และเมื่อให้แสงขาวส่องผ่านปริซึม แสงขาวจะแยกออกเป็นแสงสีรุ้งต่อเนื่องกัน เรียกว่า แถบสเปกตรัมของแสง

สเปกตรัม
สเปกตรัม หมายถึง อนุกรมของแถบสีหรือ หรือเส้นที่ได้จากการผ่านพลังงานรังสีเข้าไปในสเปกโตรสโคป ซึ่งทำให้พลังงานรังสีแยกออกเป็นแถบหรือเป็นเส้นที่มีความยาวคลื่นต่าง ๆ เรียงลำดับกันไป
สเปกตรัมของอะตอม (atomic spectrum)
คลื่นแม่เหล็กไฟฟ้าในช่วงแสงขาวประกอบด้วยแสงที่มีความยาวคลื่นหลายค่าซึ่งเราไม่สามารถแยกส่วนประกอบของคลื่นต่าง ๆ ออกจากกันด้วยตาได้ ต้องใช้เครื่องมือช่วย เช่น ปริซึม หรือสเปกโตรสโคป (spectroscope) เมื่อเราผ่านแสงสีขาวหรือแสงสีต่าง ๆ ไปยังปริซึม แสงจะแยกออกมาเป็นแถบสีต่าง ๆ เรียงกันตามความยาวคลื่น แถบสีที่แยกออกมาได้เรียกว่า สเปกตรัม
แบ่งเป็น 2 ประเภท ดังนี้
1) สเปกตรัมแบบต่อเนื่อง (continuous spectrum) จะเป็นสเปกตรัมที่ประกอบด้วยแสงที่มีความยาวคลื่นและความถี่ต่อเนื่องจนเห็นเป็นแถบ ได้แก่ สเปกตรัมของแสงขาวซึ่งจะเห็นเป็นแถบสีรุ้งเรียงต่อกัน โดยแสงสีม่วงหักเหมากที่สุด มีความยาวคลื่นสั้น แต่มีพลังงานมากที่สุด ในขณะที่แสงสีแดงจะหักเหน้อยที่สุด มีความยาวคลื่นยาวที่สุด และมีพลังงานน้อยที่สุด
2) สเปกตรัมแบบไม่ต่อเนื่องหรือแบบเส้น (Discontinuous spectrum or Line spectrum) เป็นสเปกตรัมที่ประกอบด้วยเส้นสเปกตรัมที่มีความยาวคลื่นบางค่าเว้นระยะเป็นเส้น ๆ บนพื้นดำ เนื่องจากสเปกตรัมแต่ละเส้นเป็นคลื่นแม่เหล็กไฟฟ้าเราจึงสามารถคำนวณหาค่าพลังงานของเส้นสเปกตรัมแต่ละเส้นได้จากสมการ
ความยาวคลื่น (Wavelength) l ( แลมบ์ดา ) หมายถึง ระยะทางที่คลื่นเคลื่อนที่ครบ 1 รอบพอดี มีหน่วยเป็นเมตร ( m ) หรือหน่วยย่อยของเมตร เช่น นาโนเมตร (nm) โดย 1 nm = 10^-9 เมตร

ความถี่ของคลื่น n (นิว) หมายถึง จำนวนรอบของคลื่นที่เคลื่อนที่ผ่านจุดใดจุดหนึ่งในเวลา 1 วินาที มีหน่วยเป็นจำนวนรอบต่อวินาที หรือ เฮิร์ตซ์ (Hertz) หรือ Hz
แอมปลิจูด (Amplitude) คือ ความสูงของยอดคลื่น
มักซ์ พลังค์ (Max Planck) นักวิทยาศาสตร์ชาวเยอรมัน ได้ศึกษาพลังงานของคลื่นแม่เหล็กไฟฟ้าและได้ข้อสรุปเกี่ยวกับความสัมพันธ์ระหว่างพลังงานของคลื่นแม่เหล็กไฟฟ้ากับความถี่ของคลื่นนั้นว่า พลังงานของคลื่นแม่เหล็กไฟฟ้าแปรผันตามความถี่ของคลื่นและแปรผกผันกับความยาวคลื่น ดังความสัมพันธ์ต่อไปนี้

E คือพลังงานของคลื่นแม่เหล็กไฟฟ้า มีหน่วยเป็น จูล
h คือค่าคงตัวของพลังค์ มีค่า 6.626 × 10^-34 จูลวินาที
ν คือความถี่ของคลื่นแม่เหล็กไฟฟ้า มีหน่วยเป็นเฮิรตซ์
c คือความเร็วของคลื่นแม่เหล็กไฟฟ้าในสุญญากาศ ซึ่งเท่ากับ 2.997 × 10^8 เมตรต่อวินาที(อาจใช้3.0 × 10^8 เมตรต่อวินาที)
λ คือความยาวคลื่นของคลื่นแม่เหล็กไฟฟ้า หน่วยเป็นเมตร

 |
| ตัวอย่างโจทย์ |
สเปกตรัมเกิดได้อย่างไร
สถานะพื้น (ground state)
หมายถึงอะตอมที่อิเล็กตรอนซึ่งเคลื่อนที่อยู่รอบนิวเคลียสมีพลังงานเฉพาะตัวอยู่ในระดับพลังงานต่ำ อะตอมในสถานะพื้นจะมีความเสถียรเนื่องจากมีพลังงานต่ำ
สถานะกระตุ้น (excited state)
หมายถึงอะตอมที่ได้รับพลังงานเพิ่มขึ้น ทำให้อิเล็กตรอนถูกกระตุ้นให้อยู่ในระดับพลังงานสูงขึ้น ที่สถานะกระตุ้นอะตอมจะไม่เสถียร เนื่องจากมีพลังงานสูง

อะตอมที่ได้รับพลังงาน เช่น จากการเผา หรือจากกระแสไฟฟ้า อิเล็กตรอนจะเปลี่ยนจากสถานะพื้นไปสู่สถานะกระตุ้นซึ่งไม่เสถียร จึงต้องคายพลังงานออกมา ซึ่งพลังงานที่คายออกมาจะอยู่ในรูปพลังงานแสงหรือคลื่นแม่เหล็กไฟฟ้า เมื่อผ่านปริซึมหรือสเปกโตรสโคปจะแยกแสงออกเป็นเส้นสเปกตรัม
การที่ธาตุแต่ละชนิดให้เส้นสเปกตรัมออกมาหลายเส้น แสดงว่าอิเล็กตรอนที่อยู่รอบนิวเคลียสมีหลายระดับพลังงาน ระดับพลังงานที่อยู่ใกล้นิวเคลียสจะมีพลังงานต่ำ ส่วนระดับพลังงานที่อยู่ห่างนิวเคลียสจะมีพลังงานสูง เมื่ออิเล็กตรอนคายพลังงานอาจคายพลังงานได้หลายช่วงความยาวคลื่น จึงมองเห็นเส้นสเปกตรัมได้หลายเส้น
นักวิทยาศาสตร์ได้ศึกษาสเปกตรัมของแก๊ส เพราะว่ามีอะตอมอยู่ห่างกัน และใช้อะตอมไฮโดรเจนเนื่องจากมี 1 อิเล็กตรอน พบว่ามีเส้นสเปกตรัมที่ปรากฏในช่วงความยาวคลื่นที่มองเห็นได้โดยมีความยาวคลื่น 410 , 434 , 486 และ 656 นาโนเมตร ตามลำดับ นอกจากนี้การศึกษาเส้นสเปกตรัมของอะตอมของธาตุอื่นๆ ก็พบว่าอิเล็กตรอนในอะตอมของแต่ละธาตุคายพลังงานได้บางค่า และมีเส้นสเปกตรัมเฉพาะตัวไม่ซ้ำกัน โดยเส้นสีแดงมีพลังงานต่ำสุด (3.02 x 10–22 kJ) และเส้นสีม่วงมีพลังงานสูงสุด (4.48 x 10–22 kJ)



การที่นักวิทยาศาสตร์ใช้อะตอมของไฮโดรเจนเป็นตัวอย่างในการแปลความหมายของเส้นสเปกตรัม เพราะเป็นอะตอมที่มีอิเล็กตรอนเดียว จากการทดลองหลายครั้งพบว่าอะตอมของไฮโดรเจนให้เส้นสเปกตรัมได้หลายเส้นที่มีลักษณะเหมือนกันทุกครั้ง จึงสรุปได้ว่าอิเล็กตรอนในอะตอมของไฮโดรเจนขึ้นไปอยู่ในสถานะกระตุ้นที่มีพลังงานแตะต่างกันได้หลายระดับ ค่าพลังงานของเส้นสเปกตรัมแสดงให้เห็นถึงการเปลี่ยนระดับพลังงานของอิเล็กตรอนในอะตอมจากระดับพลังงานสูงมายังระดับพลังงานต่ำ
จากข้อมูลในตาราง แสดงว่าอะตอมของไฮโดรเจนมีพลังงานหลายระดับและความแตกต่างระหว่างพลังงานของแต่ละระดับที่อยู่ถัดไปก็ไม่เท่ากัน ความแตกต่างของพลังงานจะมีค่าน้อยลงเมื่อระดับพลังงานสูงขึ้น จากเหตุผลที่อธิบายมานี้ช่วยให้สรุปได้ว่า
1) เมื่ออิเล็กตรอนได้รับพลังงานในปริมาณที่เหมาะสม อิเล็กตรอนจะขึ้นไปอยู่ในระดับพลังงานที่สูงกว่าระดับพลังงานเดิม แต่จะอยู่ในระดับใดขึ้นกับปริมาณพลังงานที่ได้รับ การที่อิเล็กตรอนขึ้นไปอยู่ในระดับพลังงานใหม่ทำให้อะตอมไม่เสถียร อิเล็กตรอนจะกลับมาอยู่ในระดับพลังงานที่ต่ำกว่า ซึ่งในการเปลี่ยนตำแหน่งนี้อิเล็กตรอนจะคายพลังงานออกมา การดูดหรือคายพลังงานจะต้องมีค่าเฉพาะตามทฤษฎีของพลังค์ โดยค่าต่ำสุดจะเท่ากับความถี่ของอิเล็กตรอนนั้นคูณด้วยค่าคงที่ของพลังค์
2) การเปลี่ยนระดับพลังงานของอิเล็กตรอนไม่จำเป็นต้องเปลี่ยนไปยังระดับพลังงานที่อยู่ติดกันอาจมีการเปลี่ยนข้ามระดับได้ แต่เมื่ออิเล็กตรอนรับพลังงานแล้วจะขึ้นไปอยู่ระหว่างระดับพลังงานไม่ได้ จะต้องขึ้นไปอยู่ในระดับใดระดับหนึ่งเสมอ
3) ผลต่างของพลังงานระหว่างระดับพลังงานต่ำจะมีค่ามากกว่าผลต่างของพลังงานระหว่างระดับพลังงานที่สูงขึ้นไป
สรุปการเกิดสเปกตรัม
1) การตรวจหาสเปกตรัม ถ้าเป็นสารประกอบทำโดย การเผาสารประกอบถ้าเป็นก๊าซทำโดย นำก๊าซมาบรรจุในหลอดแก้ว แล้วปรับความดันให้ต่ำแล้วใช้พลังงานไฟฟ้าแทนการเผา
2) สีเปลวไฟ หรือสเปกตรัม เกิดจากสาเหตุเดียวกัน ข้อแตกต่าง คือ
สีเปลวไฟ เป็นสีที่มองจากตาเปล่า จะเห็นเป็นสีเดียว ซึ่งเป็นสีที่เด่นชัดที่สุด
สีสเปกตรัมเป็นสีที่ใช้เครื่องมือ สเปกโตรสโคป ส่องดูเปลวไฟ จะเห็นเป็นเส้นสเปกตรัมหลายเส้น และความเข้มมากที่สุดจะเป็นสีเดียวกันกับสีของเปลวไฟ
3) สีของเปลวไฟ หรือสีของสเปกตรัมเป็นสีที่เกิดที่เกิดจากส่วนที่เป็นไอออนของโลหะ หรือไอออนบวกนั่นเอง ดังเช่น
Li+ สีแดง , Na+ สีเหลือง , K+ สีม่วง , Ca2+ สีแดงอิฐ ,
Ba2+ สีเขียวอมเหลือง , Cu2+ สีเขียว
4) ธาตุแต่ละธาตุมีเส้นสเปกตรัมเป็นลักษณะเฉพาะตัวไม่ซ้ำกัน
ลักษณะเเบบจำลองอะตอมของโบว์
จากความรู้เรื่องสเปกตรัม นีลส์ โบว์ ได้เสนอแบบจำลองขึ้นมาใหม่โดยปรับปรุงแบบจำลองอะตอมของรัทเทอร์ฟอร์ด เพื่อให้เห็นลักษณะของอิเล็กตรอนที่อยู่รอบ ๆ นิวเคลียส เป็นวงคล้ายกับวงโคจรของดาวเคราะห์รอบดวงอาทิตย์ ดังรูป


สรุปแบบจำลองอะตอมของโบว์
1) อิเล็กตรอนจะอยู่เป็นชั้น ๆ แต่ละชั้นเรียกว่า “ ระดับพลังงาน ”
2) แต่ละระดับพลังงานจะมีอิเล็กตรอนบรรจุได้ดังนี
จำนวนอิเล็กตรอน = 2n^2
3) อิเล็กตรอนที่อยู่ในระดับพลังงานนอกสุดเรียกว่า เวเลนซ์อิเล็กตรอน ( Valence electron ) จะเป็นอิเล็กตรอนทีเกิดปฏิกิริยาต่าง ๆ ได้
4) อิเล็กตรอนที่อยู่ในระดับพลังงานวงใน อยู่ใกล้นิวเคลียสจะเสถียรมาก เพราะประจุบวกจากนิวเคลียสดึงดูด เอาไว้อย่างดี ส่วนอิเล็กตรอนระดับพลังงานวงนอกจะไม่เสถียรเพราะนิวเคลียสส่งแรงไปดึงดูดได้น้อยมาก จึงทำให้อิเล็กตรอนเหล่านี้หลุดออกจากอะตอมได้ง่าย
5) ระดับพลังงานวงในจะอยู่ห่างกันมาก ส่วนระดับพลังงานวงนอกจะอยู่ชิดกันมาก
6) การเปลี่ยนระดับพลังงานของอิเล็กตรอน ไม่จำเป็นต้องเปลี่ยนในระดับถัดกัน อาจเปลี่ยนข้ามระดับพลังงานก็ได้

โครงสร้างอะตอมตามแบบจำลองอะตอมแบบกลุ่มหมอกยังไม่ใช่ข้อยุติในการศึกษาทดลองเกี่ยวกับอะตอม เพราะความรู้ทางวิทยาศาสตร์มีการพัฒนาอย่างต่อเนื่องตลอดเวลา ดังนั้นในอนาคตจึงอาจมีแบบจำลองอะตอมแบบอื่นตามข้อมูลที่ค้นพบใหม่
รูปทรงต่างๆของกลุ่มหมอกอิเล็กตรอน จะขึ้นอยู่กับระดับพลังงานของอิเล็กตรอน การใช้ทฤษฎีควันตัม จะสามารถอธิบายการจัดเรียงตัวของอิเล็กตรอนรอบนิวเคลียส ได้ว่าอิเล็กตรอนจัดเรียงตัวเป็นออร์บิทัล(orbital) ในระดับพลังงานย่อย s , p , d , f แต่ละออร์บิทัล จะบรรจุอิเล็กตรอนเป็นคู่ ดังนี้
s – orbital มี 1 ออร์บิทัล หรือ 2 อิเล็กตรอน
p – orbital มี 3 ออร์บิทัล หรือ 6 อิเล็กตรอน
d – orbital มี 5 ออร์บิทัล หรือ 10 อิเล็กตรอน
f – orbital มี 7 ออร์บิทัล หรือ 14 อิเล็กตรอน
แต่ละออร์บิทัลจะมีรูปร่างลักษณะแตกต่างกัน ขึ้นอยู่กับการเคลื่อนที่ของอิเล็กตรอนในออร์บิทัล และระดับพลังงานของอิเล็กตรอนในออร์บิทัลนั้นๆ เช่น
s – orbital มีลักษณะเป็นทรงกลม
p – orbital มีลักษณะเป็นกรวยคล้ายหยดน้ำ ลักษณะแตกต่างกัน 3 แบบ ตามจำนวนอิเล็กตรอนใน 3 ออร์บิทัล คือ Px , Py , Pz
d – orbital มีลักษณะและรูปทรงของกลุ่มหมอก แตกต่างกัน 5 แบบ ตามจำนวนอิเล็กตรอนใน 5 ออร์บิทัล คือ dx2-y2 , dz2 , dxy , dyz , dxz
เป็นแบบจำลองที่นักวิทยาศาสตร์คิดว่าเป็นไปได้มากที่สุดทั้งนี้ได้จากการประมวลผลการทดลองและข้อมูลต่างๆ อะตอมภายหลังจากที่นีลส์โบร์ ได้เสนอแบบจำลองอะตอมขึ้นมา อาจสรุปได้ดังนี้
1) อิเล็กตรอนไม่สามารถวิ่งรอบนิวเคลียสด้วยรัศมีที่แน่นอน บางครั้งเข้าใกล้บางครั้งออกห่าง จึงไม่สามารถบอกตำแหน่งที่แน่นอนได้ แต่ถ้าบอกได้แต่เพียงที่พบอิเล็กตรอนตำแหน่งต่างๆภายในอะตอมและอิเล็กตรอนที่เคลื่อนที่เร็วมากจนเหมือนกับอิเล็กตรอนอยู่ทั่วไป ในอะตอมลักษณะนี้เรียกว่า " กลุ่มหมอก"
2) กลุ่มหมอกของอิเล็กตรอนในระดับพลังงานต่างๆจะมีรูปทรงต่างกันขึ้นอยู่กับจำนวนอิเล็กตรอน และระดับพลังงานอิเล็กตรอน
3) กลุ่มหมอกที่มีอิเล็กตรอนระดับพลังงานต่ำจะอยู่ใกล้นิวเคลียสส่วนอิเล็กตรอนที่มีระดับพลังงานสูงจะอยู่ไกลนิวเคลียส
4) อิเล็กตรอนแต่ละตัวไม่ได้อยู่ในระดับพลังงานใดพลังงานหนึ่งคงที่
5) อะตอมมีอิเล็กตรอนหลายๆระดับพลังงาน

ในปีพ.ศ. 2429 ออยเกน โกลด์ชไตน์(Eugen Goldstein) ได้ทำ การดัดแปลงหลอดรังสีแคโทด โดยการสลับตำแหน่งของแคโทดและแอโนด ดังรูป ซึ่งเมื่อผ่านกระแสไฟฟ้าเข้าไปพบว่า ฉาก เกิดการเรืองแสง แสดงว่ามีรังสีออกจากแอโนด ซึ่งโกลด์ชไตน์เรียกรังสีชนิดนี้ว่า รังสีแคแนล (canal ray) หรือรังสีแอโนด (anode ray) ซึ่งมีประจุบวก
 |
| หลอดรังสีเเคโทดที่ดัดเเปลง |


 |
| สัญลักษณ์นิวเคลียร์ |
 |
| ตัวอย่าง |



 |
| ตัวอย่างธาตุที่เป็นไอโซโทป ไอโซโทน ไอโซบาร์ ไอโซอิเล็กทรอนิก |

สูตรจริง
n = 1 2
n = 2 8
n = 3 18
n = 4 32
n = 5 32
n = 6 18
n = 7 8
หลักการจัดเรียงอิเล็กตรอน
1) จะต้องจัดเรียงอิเล็กตรอนเข้าในระดับพลังงานต่ำสุดให้เต็มก่อน จึงจัดให้อยู่ระดับพลังงานถัดไป
2) เวเลนซ์อิเล็กตรอนจะเกิน 8 ไม่ได้
3) จำนวนอิเล็กตรอนในระดับพลังงานถัดเข้าไปของธาตุในหมู่ IA , IIA เท่ากับ 8 ส่วนหมู่ IIIA – VIIIA เท่ากับ 18
การจัดอิเล็กตรอน มีความสัมพันธ์กับการจัดหมู่และคาบอย่างไร
1) เวเลนซ์อิเล็กตรอน จะตรงกับเลขที่ของหมู่ ดังนั้น ธาตุที่อยู่หมู่เดียวกันจะมีเวเลนซ์อิเล็กตรอนเท่ากัน
2) จำนวนระดับพลังงาน จะตรงกับเลขที่ของคาบ ดังนั้น ธาตุในคาบเดียวกันจะมีจำนวนระดับพลังงานเท่ากัน เช่น 35Br มีการจัดเรียงอิเล็กตรอนดังนี้ 2 , 8 , 18 , 7 ดังนั้น Br จะอยู่ในหมู่ที่ 7 เพราะมีเวเลนซ์อิเล็กตรอน 7 และอยู่ในคาบที่ 4 เพราะมีจำนวนระดับพลังงาน 4
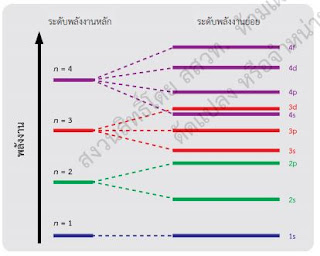
 |
| เเผนภาพระดับพลังงานที่เเสดงจำนวนออร์บิทัล |

จากตาราง จะเห็นว่าจำนวนอิเล็กตรอนสูงสุดในระดับพลังงานย่อย s p d และ f มีค่าเท่ากับ 2 6 10 และ 14 ตามลำดับ แต่เนื่องจากพลังงานย่อย s p d และ f มี 1 3 5 และ 7 ออร์บิทัลตามลำดับ แสดงว่า 1 ออร์บิทัลสามารถบรรจุอิเล็กตรอนได้ 2 อิเล็กตรอน
 |
| เเผนภาพเเสดงลำดับการบรรจุอิเล็กตรอนในออร์บิทัลต่างๆ |
จากแผนภาพสามารถเรียงลำ ดับพลังงานได้ดังนี้
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p …
ไฮโดรเจนอะตอมซึ่งมี 1 อิเล็กตรอน สามารถเขียนสัญลักษณ์แสดงการจัดเรียงอิเล็กตรอนได้เป็น 1s¹ โดยมีความหมายดังนี้
 |
| สัญลักษณ์เเสดงการจัดเรียงอิเล็กตรอนของไฮโดรเจนอะตอม |

- ธาตุที่อยู่ในแนวนอนเดียวกัน เรียกว่า อยู่ใน คาบ เดียวกัน
ในระหว่างปี พ.ศ. 2346 ถึง 2456 มีธาตุต่าง ๆที่พบในธรรมชาติประมาณ 63 ธาตุ ซึ่งนักวิทยาศาสตร์ได้พยายามจัดธาตุเหล่านี้ให้เป็นหมวดหมู่หรือเป็นตารางธาตุโดยในช่วงแรก ๆ นั้นแบ่งธาตุออกเป็นหมวดหมู่โดยอาศัยสมบัติของธาตุ ทั้งนี้ได้จากการสังเกตพบความคล้ายคลึงกันของสมบัติของธาตุเป็นกลุ่ม ๆ ทำให้นำมาจัดเป็นตารางธาตุได้ เช่นแบ่งกลุ่มโดยอาศัยสมบัติเกี่ยวกับโลหะ-อโลหะ โดยอาศัยสมบัติของความเป็นกรด-เบสของธาตุ เป็นต้น ต่อมาเมื่อหามวลอะตอมของธาตุได้ จึงใช้มวลอะตอมมาประกอบในการจัดตารางธาตุ จนในปัจจุบันจัดตารางธาตุโดยอาศัยการจัดเรียงอิเล็กตรอน




- หมู่ IA เรียกว่า โลหะแอลคาไล (Alkali metal)[1] ได้แก่ Li Na K Rb Cs Fr
- หมู่ IIA เรียกว่า โลหะแอลคาไลน์เอิร์ท (Alkaline earth metal) ได้แก่ Be Mg Ca Sr Ba Ra
- หมู่ VIIA เรียกว่า ธาตุแฮโลเจน (Halogen) ได้แก่ F Cl Br I At
- หมู่ VIIIA เรียกว่า แก๊สเฉื่อย (Inert gas) หรือแก๊สมีตระกูล (Noble gas) ได้แก่ He Ne Ar Kr Xe Rn
- คาบที่ 1 มี 2 ธาตุ คือ H และ He
- คาบที่ 2 มี 8 ธาตุ คือ Li จนถึง Ne
- คาบที่ 3 มี 8 ธาตุ คือ Na จนถึง Ar
- คาบที่ 4 มี 18 ธาตุ คือ K จนถึง Kr
- คาบที่ 5 มี 18 ธาตุ คือ Rb จนถึง Xe
- คาบที่ 5 มี 18 ธาตุ คือ Rb จนถึง Xe
- คาบที่ 6 มี 32 ธาตุ คือ Cs ถึง Rn
- คาบที่ 7 มี 29 ธาตุ(ที่ค้นพบ) คือ Fr จนถึง Ds และ Uuu Uub Uuq Uuh Uuo


เมื่อพิจารณาขนาดอะตอมของธาตุที่อยู่ในคาบเดียวกันพบว่า ขนาดอะตอมมีแนวโน้มลดลง เมื่อเลขอะตอมเพิ่มขึ้น อธิบายได้ว่าเนื่องจากธาตุในคาบเดียวกันมีเวเลนซ์อิเล็กตรอนอยู่ในระดับ พลังงานเดียวกัน แต่มีจำ นวนโปรตอนในนิวเคลียสแตกต่างกัน ธาตุที่มีจำ นวนโปรตอนมากจะดึงดูด เวเลนซ์อิเล็กตรอนด้วยแรงที่มากกว่าธาตุที่มีจำ นวนโปรตอนน้อย เวเลนซ์อิเล็กตรอนจึงเข้าใกล้ นิวเคลียสได้มากกว่าทำ ให้อะตอมมีขนาดเล็กลง
 |
| รูป 2.22 รัศมีไอออนของ Mg^2+ และ O^2- |
 |
| รูป 2.23 เปรียบเทียบขนาดของอะตอมกับไอออน |

2.4.5 พลังงานไอออไนเซซัน

 |
| สำหรับพลังงานไอออไนเซชันของธาตุ20 ธาตุแรกเรียงตามเลขอะตอมแสดงไว้ในตาราง 2.10 |
 |
| ตาราง 2.10 (ขยายใหญ่เพื่อดูชัดๆ) |

 |
| รูป 2.26 ค่าพลังงานไอออไนเซชันลำดับที่ 1 ของธาตุบางชนิด |


 |
| รูป 2.27 ค่าสัมพรรคภาพอิเล็กตรอนของธาตุบางชนิด |
เมื่อพิจารณาตามคาบพบว่า ค่าสัมพรรคภาพอิเล็กตรอนของธาตุอโลหะ (ยกเว้นธาตุหมู่VIIIA) มีค่ามากกว่าธาตุโลหะ แสดงว่าธาตุอโลหะมีแนวโน้มที่จะรับอิเล็กตรอนได้ดีกว่าธาตุโลหะ เมื่อพิจารณา โดยภาพรวมทั้งหมดจะพบว่าธาตุหมู่ VIIA มีค่าสัมพรรคภาพอิเล็กตรอนสูงที่สุดแสดงว่ามีแนวโน้มใน การรับอิเล็กตรอนได้ดีกว่าธาตุหมู่อื่น ที่เป็นเช่นนี้อาจอธิบายได้ว่าการรับ 1 อิเล็กตรอนของธาตุในหมู่ นี้จะทำ ให้อะตอมมีการจัดเรียงอิเล็กตรอนเหมือนธาตุหมู่ VIIIA หรือแก๊สมีสกุลซึ่งมีความเสถียรมาก
 |
| รูป 2.28 ค่าอิเล็กโทรเนกาติวิตีของธาตุบางชนิด |

 |
| รูป 2.29 ธาตุแทรนซิชัน |


 |
| รูป 2.31 การแผ่รังสีของไอโซโทปกัมมันตรังสีผ่านสนามไฟฟ้า |


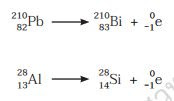

 |
| รูป 2.32 เขตเสถียรภาพของไอโซโทปของธาตุและชนิดของรังสีที่แผ่นอกเขตเสถียรภาพ |
 |
| รูป 2.33 ปริมาณรังสีที่ได้รับในแต่ละวันโดยประมาณ |
 |
| รูป 2.34 สัญลักษณ์รังสี |
 |
รูป 2.35 สัญลักษณ์รังสีแบบใหม่ |

 |
 |
| รูป 2.36 แสดงปริมาณของ Na-24 ที่ลดลงครึ่งหนึ่งทุก ๆ 15 ชั่วโมง |






 |
| แสดงปริมาณของ Na-24 ที่ลดลงครึ่งหนึ่งทุก ๆ 15 ชั่วโมง |









ไม่มีความคิดเห็น:
แสดงความคิดเห็น